지난 해 tisagenlecleucel (KYMRIAH™)와 axicabtagene ciloleucel (YESCARTA™) 의 승인을 받아, 키메라 항원 수용체 (CAR) T세포 치료는 특정 혈액암 환자 치료의 패러다임을 바꿔놓았다.
CAR T 세포 치료란?
CAR T-세포 치료는 환자 자신의 T 세포가 암을 인식하고 근절할 수 있도록 하는 재설계를 포함한다. 이 T세포는 유전적으로 변형되어 인공 수용체를 표현하고 특정 항원과 결합하여 환자의 종양 세포를 죽일 수 있게 된다. T 세포 수용체 매개 면역 반응과 달리, CAR T 세포 매개 면역 반응은 세포 밖 종양 관련 항원의 직접적인 인지로 이어진다. 하지만, 면역성은 어려워질 수 있다.
그림1. 정상 vs. CAR T-세포[1]
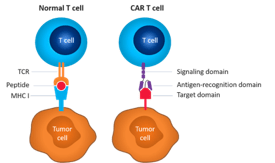
이미지출처: Locke, F. L., MD, Gardner, R., MD, & Neelapu, S. S., MD. (2017, December 20). Test Driving CARs: Optimizing Outcomes. Retrieved from https://www.medscape.org/viewarticle/890215_transcript
CAR T 세포 치료 개발
지금까지, 두 가지의 CAR T 세포 치료가 FDA에 의해 승인 되었다.
- Tisagenlecleucel. 재발 혹은 널리 퍼진 난치 B 세포 미만성 림프종을 앓는 어른과 재발 혹은 다루기 힘든 급성 림프구성 백혈병을 앓는 25세 이하의 성년을 치료하기 위해 승인됨.
- Axicabtagene ciloleucel. 두 가지 이상의 전신 요법에 반응했거나 재발한 특정 유형의 B 세포 림프종을 앓는 어른 치료를 위해 승인됨.
CAR T 세포 치료의 임상 경로 개발은 지난 몇 십년 간 2018년 8월 기준 미국에서만 144개의 임상이 진행 중이며 유의미하게 가속화했다.[2]
그림 2. 미국과중국의 CAR T 세포임상실험2
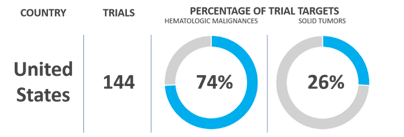
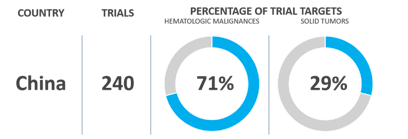
자료및이미지출처: The-Scientist.com. Cell and Gene Therapy Tracker: Global CAR T-Cell Trials. Infographic created with data compiled by CellTrials.org.
최근 몇 년 간, 연구원들은 치료법을 보다 안전하게 만들기 위해 CAR T세포 구조 개선 (그림 3 참조) 혹은 (suicide switch와 같은) 매커니즘 개발 등CAR T 세포 치료의 효능 강화를 위한 노력을 기했다.
그림3. CAR T 세포설계의진화[3]
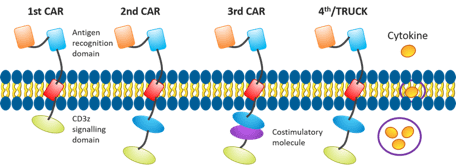
이미지출처: Xu D, et al. The development of CAR design for tumor CAR-T cell therapy. Oncotarget 2018;9(17):13991-14004.
CAR T 세포 치료의 이점 및 약점 [4],[5],[6]
CAR T 세포 치료에는 다른 면역항암제 치료와 비교했을 때 여러 이점이 존재한다.
- HLA 독립 항원 인식, 보편적 적용 가능
- 특정 T 세포 특수형의 선택적 수정
- 종양 특이 T 세포의 빠른 생성
- 이식편 숙주 반응의 최소 위험
- 살아있는 “약물”로, 단일 투약 후에도 지속되는 면역 가능성
- CAR 구성의 추가 수정 능력
그러나, CAR T 세포 치료는 여러 어려움과도 관련이 있다.
- 비싼 가격
- T 세포 처리 및 수정에 필요한 시간
- 사이토카인 과다 방출 증후군, 종양용해증후군 및 신경학상 독성을 포함하는 부작용
- 목표 정확, 종양 독성 부정확 (on-target , off-tumor toxicity) (예: B 세포 무형성)
- 목표 부정확, 종양 독성 부정확 (Off-target, off-tumor toxicity) (예: 감마글로불린혈증)
사이토카인 방출 증후군 (CRS)
최근 임상 실험에서 보고된 CRS 발생률은 50~93%이며[7], 증상은 독감처럼 미미하거나 목숨을 위협할 정도의 전신성 염증반응 증후군을 수반한다. 현재 경쟁적으로 인터류킨 6 (IL-6)의 수용체와의 결합을 억제하고 IL-6가 염증 전 효과[8]를 가하는 것을 방해하는 단일 클론 항체 tocilizumab는 경감하는 경미하거나 심한 CRS를 관리하는 일선 치료법으로 간주된다. Tocilzumab이 효과를 보지 못하는 경우에는 스테로이드를 사용했다. 인간화된 면역 글로불린 항체 (IG) 항인간 면역 글로불린 항체 (anti-hIL)-6R또한 2017년 8월 미국 FDA로부터 CRS 치료 승인을 받았다. 지금까지 tocilizumab 을 이용한 예방은 CRS의 발생을 감소시키지 못했다.
견고한 종양 징후로의 성공적인 확장에 있어 향후 CAR T 세포 치료
다음 핵심 임상 질문에 답하고자 하는 연구원들의 노력과 함께 향후에도 CAR T 세포 치료에 지속되는 투자를 예상한다.
- CAR T 세포 치료는 치료 초반에 사용될 수 있는가?
- CAR T 세포 치료는 자기 조직 이식을 대체할 수 있는가?
- 유지에 있어 CAR T 세포의 역할은 무엇인가?
- CAR T 세포 치료가 어떻게 더욱 안전해질 수 있는가?
- CAR T 세포 치료가 기성화될 수 있는가?
현재 진행 중인 연구와 함께, 개선된 안전성을 동반한 기성품의 사용으로 CAR T 세포 치료의 접근성과 가격합리성을 높여, 이를 필요로하는 환자들에게 더욱 빠르고 비용 효율적인 제조 및 세포 확장을 이룩할 수 있기를 기대한다.
